Ученые и молодые специалисты Московского государственного университета имени М.В. Ломоносова совершили выдающееся открытие, пролив свет на процессы, происходящие с рибосомой в промежутках между актами создания новых белков. До недавнего времени на мировом научном горизонте существовало лишь два известных состояния рибосом: ассоциированное — когда рибосома работает, синтезируя белковые цепочки, и диссоциированное — когда она разделяется на две части и временно неактивна. Как именно осуществляется переход между этими двумя состояниями, ранее оставалось малоизученным. Но сотрудники МГУ неожиданно выявили еще одно промежуточное состояние рибосом, что стало новым шагом в познании молекулярных механизмов клеточной жизни. Данный научный прорыв поддержан Российским научным фондом (РНФ) и открывает двери для поиска новых инновационных антибиотиков.
Строение и функция рибосомы: ключевой элемент клеточной деятельности
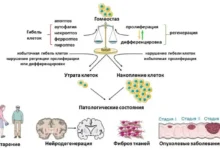
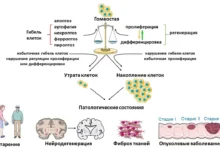
Рибосома — это уникальный и сложный молекулярный аппарат, состоящий из белков и рибонуклеиновой кислоты, который отвечает за создание белков из аминокислот в клетке. Рибосомы формируются из двух частей: малой и большой субъединиц. После завершения задачи по созданию новой белковой молекулы у бактерий происходит распад рибосомы на эти субъединицы, процесс называется диссоциацией. Именно в таком виде они не способны продолжать работу, пока не соединятся снова — процесс называется ассоциацией. Таким образом, баланс между этими состояниями обеспечивает динамику роста и нормального функционирования клетки.
IF3 и его роль в работе рибосомы
В поддержке разобранного (диссоциированного) состояния рибосомы ключевую роль играет специализированный белок IF3 (Initiation Factor 3 или 3-й фактор инициации трансляции). IF3 связывается с малой субъединицей рибосомы, препятствуя её преждевременному соединению с большой субъединицей. Такой механизм обеспечивает качественную подготовку к новому раунду синтеза белка. Пока IF3 удерживает малую субъединицу в свободном состоянии, рибосома не может приступить к работе — это вынужденная пауза, необходимая для оптимального контроля биосинтетических процессов.
Неожиданные промежуточные этапы в диссоциации рибосом
Ранее было неясно, каким образом происходит разделение рибосомы на две части и изменяется ли её структура в процессе перехода. Исследовательская группа МГУ впервые смогла обнаружить уникальные переходные стадии между целой и разобранной рибосомой у бактерий. Такой промежуточный этап открывает новые горизонты для детального понимания работы клеточных механизмов и может стать ключом к новым стратегиям терапии, в особенности в области разработки антимикробных препаратов.
Исследование Петра Каменского: от митохондрий к бактериям
Профессор Петр Каменский, выдающийся специалист биологического факультета МГУ, рассказывает, что это открытие произошло во многом благодаря удачному стечению обстоятельств. Исследователи занимались анализом процессов трансляции в митохондриях, где также присутствует собственная рибосомальная система для синтеза белков. Для проверки гипотезы ученые решили выяснить, может ли белок mtIF3 (митохондриальный 3-й фактор инициации трансляции из пекарских дрожжей) замещать бактериальный IF3 в клетках кишечной палочки E. coli.
Для этого в бактериальный геном E. coli был внедрен ген митохондриального аналога IF3. Далее специалисты наблюдали за ростом мутантных бактериальных клеток, чтобы понять, насколько эффективно mtIF3 справляется с задачей организации работы рибосомы в чужеродных для себя условиях. Результаты эксперимента оказались значимыми и подтвердили, что митохондриальный фактор способен в некоторой степени замещать бактериальный IF3, открывая новые аспекты в изучении универсальности механизмов трансляции у разных форм жизни.
Влияние открытия и перспектива развития новых технологий
Найденное промежуточное состояние между ассоциацией и диссоциацией рибосомы расширяет возможности для фундаментальных исследований по регулированию синтеза белка. Углубленное понимание того, как работает IF3 и подобные белки в бактериях и митохондриях, способно привести к появлению новых подходов в борьбе с резистентными микроорганизмами и различными заболеваниями. Команда МГУ при поддержке Российского научного фонда способствует развитию передовой науки и вселяет уверенность в появление новых терапевтических стратегий уже в ближайшем будущем. Такие работы подчеркивают значимость фундаментальных исследований для создания инновационных методов заболевания и улучшения качества жизни человека.
Недавно коллектив учёных провёл уникальное исследование с участием кишечной палочки E. coli, изучая замену её гена IF3 на митохондриальный аналог mtlF3, взятый из дрожжей. Первый сценарий эксперимента подразумевал, что мутантные бактерии с новой версией IF3 смогут вести себя как контрольные немутантные штаммы. Альтернативное развитие событий, при котором бактерии с изменённым геном ведут себя аналогично клеткам, полностью лишённым IF3, говорило бы о невозможности такой замены. Целью эксперимента было выяснить, способен ли митохондриальный mtlF3 полноценно заменять бактериальный IF3 в клетках.
Неожиданные результаты эксперимента
Однако итоговые наблюдения учёных удивили и поставили перед ними новые вопросы. Мутантные варианты бактерий, у которых отсутствовал IF3, но присутствовал mtIF3, росли заметно хуже даже по сравнению с бактериями, у которых вообще не было IF3. Это позволило предположить, что белок, появляющийся на основе митохондриального гена из дрожжей, проявляет нежелательную токсичность для клетки бактерии. Такой результат стал неожиданным открытием и потребовал детального изучения причин возникновения токсичности.
Гипотеза о механизме токсичности
Научный интерес к этой необычной ситуации подтолкнул участников проекта к подробному рассмотрению возможных причин токсического эффекта. Как отметил профессор Пётр Каменский, в рамках обследования была предложена версия, что причина кроется в специфике биосинтеза белка и механизмах взаимодействия рибосомных субъединиц. Основная функция белка IF3 — участие в процессах разделения и объединения рибосомных компонентов. Специально для этого эксперимента из обычных бактерий были выделены рибосомы, к которым по отдельности добавляли IF3 или mtIF3. Результаты показали: введение бактериального IF3, как ожидалось, приводило к появлению исключительно отдельных субъединиц рибосомы — целые рибосомы не образовывались. Зато введение митохондриального аналога приводило к обнаружению промежуточной структуры, где субъединицы рибосомы только начали отделяться друг от друга и ещё не завершили процесс диссоциации.
Открытие нового состояния рибосомы
Дальнейшее изучение с использованием биохимических подходов позволило предположить существование уникального, ранее не описанного промежуточного состояния рибосомы. Таким образом, помимо давно известных ассоциированных и полностью диссоциированных форм рибосомы, теперь есть подтверждение о третьем переходном состоянии. Для более точного подтверждения открытия потребуется привлечение современных методов прямого наблюдения молекул — рентгеноструктурного анализа или криоэлектронной микроскопии. Благодаря им можно будет увидеть взаимное расположение атомов с исключительно высокой точностью и получить трёхмерную модель наблюдаемой структуры.
Перспективные возможности в поиске новых антибиотиков
Если в дальнейшем удастся точно охарактеризовать промежуточное рибосомное состояние, это открытие поможет заложить основы для разработки принципиально новых видов антибиотиков. В современном мире актуальна проблема устойчивости к традиционным антибиотикам: многие бактерии имеют врождённую или приобретённую резистентность к существующим препаратам. Открытие новых мишеней для воздействия на патогены становится особенно важным шагом вперёд в области молекулярной биологии. Изучение структурных особенностей рибосомы и связанных с ней биохимических процессов даёт учёным шанс создавать эффективные средства борьбы с инфекциями, против которых старые антибиотики уже не работают.
Этот проект демонстрирует, как фундаментальное научное любопытство может привести к открытиям с огромным прикладным потенциалом, открывая для науки и медицины новые горизонты.
Информация предоставлена пресс-службой МГУ
Биологи из МГУ случайно открыли, каким образом происходит разрушение рибосом — важнейших структурных элементов клетки, отвечающих за синтез белков. Этот новый взгляд на процесс позволил ученым по-новому взглянуть на фундаментальные механизмы жизнедеятельности. Оказалось, что в некоторых условиях рибосомы могут самопроизвольно разрушаться на отдельные компоненты, что открывает пути для изучения механизмов старения и развития различных болезней.
Открытие, изменившее представление о клеточной биологии
Исследование открыло перед научным сообществом новые горизонты: теперь становится возможным разработать инновационные методы контроля за функционированием рибосом. Возможно появление новых подходов к лечению заболеваний, связанных с нарушениями синтеза белка. Например, знания о поведении рибосом приведут к лучшему пониманию процессов старения и развитию лекарственных средств на клеточном уровне.
Значение исследования для науки
Это открытие стало настоящим прорывом в молекулярной биологии, ведь понимание работы рибосом позволяет точнее диагностировать и предотвращать сбои в их функционировании. Перспективы настолько велики, что с каждым днем ученые все ближе подходят к созданию технологий, повышающих качество и продолжительность жизни человека. Позитивное влияние такого открытия сложно переоценить, ведь каждый шаг в изучении клеточных механизмов открывает новые возможности для медицины и биотехнологий.
Источник: scientificrussia.ru